- 텍스트 축소
- 확대
솔젠트, 코로나19 진단시약 2개 제품 유럽인증 획득
- 송고 2020.03.02 09:49 | 수정 2020.03.02 10:29
- 동지훈 기자 (jeehoon@ebn.co.kr)
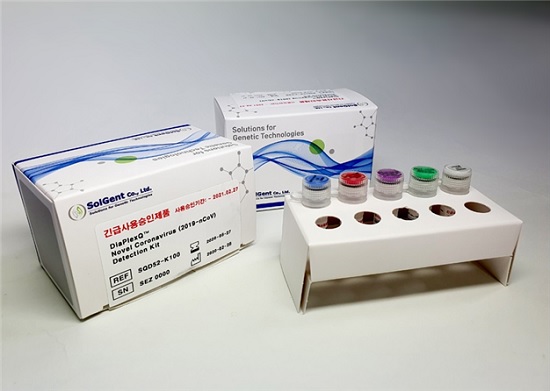
ⓒ솔젠트
솔젠트는 자체 개발한 2개의 코로나19 진단시약이 유럽인증(CE)을 획득했다고 2일 밝혔다.
CE는 진단시약 수출 시 유럽을 포함한 대부분의 국가에서 요구되는 인증이다. 지난달 질병관리본부의 긴급사용 승인으로 국내에 코로나19 진단시약의 공급이 가능해진 솔젠트는 이번 CE 획득으로 전 세계에 코로나19 진단시약을 공급할 수 있는 활로를 개척했다고 강조했다.
이번에 솔젠트가 CE를 획득한 진단시약 제품은 'DiaPlexQ Novel Coronavirus (2019-nCoV) Detection Kit'와 'DiaPlexQ 2019-nCoV (RdRp, E, N) Detection Kit' 등 두 개다.
DiaPlexQ Novel Coronavirus Detection Kit는 국내 긴급사용 승인을 받은 제품으로 2개의 코로나19 바이러스 유전자(ORF1a gene, N gene)를 RNA 추출 후 2시간 이내 동시에 정성 검출할 수 있다.
솔젠트는 긴급사용 승인을 받은 만큼 적은 양의 샘플로도 검출이 가능한 높은 민감도와 코로나19 외 다른 바이러스 및 균에서는 검출되지 않아 코로나19만을 정확히 검출할 수 있는 높은 특이도를 갖고 있다고 설명했다. 또한 상용화 된 대부분의 Real-Time PCR 장비에 호환되도록 설계됐다고 부연했다.
DiaPlexQ 2019-nCoV Detection Kit 제품은 3개의 코로나19 바이러스 유전자(RdRp gene, E gene, N gene)를 검출유전자로 하며, 이 역시 RNA 추출 후 2시간 이내 동시에 정성 검출할 수 있다.
석도수 솔젠트 공동대표는 "질병관리본부의 긴급사용 승인에 이은 CE 획득으로 기술력을 인정받았는데, 코로나19 유전자에 대한 다수의 국제 프로토콜 중 가장 특이도가 높은 유전자만을 선별하여 밤낮으로 개발한 노력의 결실"이라며 "솔젠트의 일일 생산가능물량은 1만5000~2만 테스트 규모로서 비상생산체제를 가동해 국내외 코로나19 확산 예방에 도움이 될 수 있도록 앞장서겠다"고 말했다.
유재형 공동대표는 "긴급사용 승인에 이은 CE 획득으로 국내 및 해외에도 안정적인 검사시약 공급에 일조를 하게 돼 기쁘게 생각한다"며 "대규모 발주를 논의 중이며, 최근 일본과 중동, 유럽, 동남아시아, CIS 등 20여 개 국가과 계약이 이뤄져 다음주부터 순차적으로 발송할 예정"이라고 밝혔다.
©(주) EBN 무단전재 및 재배포 금지
관련기사
전체 댓글 0
서울미디어홀딩스
패밀리미디어 실시간 뉴스





![[Beauty & Now] LG생활건강 더후, 中징둥닷컴 ‘스타어워즈’ 수상 등](https://cdnimage.ebn.co.kr/news/news-p.v1.20240417.7c7c287334004a249294890e932ce84d_T1.jpg)
![[EBN 칼럼] 한국사회투자 ‘투자자가 선호하는 스타트업’](https://cdnimage.ebn.co.kr/news/news-p.v1.20240408.84e6c000ae9c46aba86886490063ffc6_T1.jpeg)